在自然界中,没有任何生命是一座孤岛。从土壤中的微生物到浩瀚海洋里的鱼群,从人体内的肠道菌群到热带雨林中的参天大树,物种之间无时无刻不在进行着复杂的相互作用。一个长期困扰科学界的根本问题是:当不同物种彼此影响时,这种“相互作用”本身是否也镌刻在基因之中?是什么遗传机制让生命能够感知并响应其他物种的存在,从而改变自身的行为和特征?
近日,一项由上海数学与交叉学科研究院、北京雁栖湖应用数学研究院、北京林业大学等机构联合完成的开创性研究,为这个困扰生态学与进化生物学多年的“黑箱”带来了突破性答案。通讯作者邬荣领教授及其团队在国际上首次构建了一套计算生态遗传模型(Horizontally Interactive Epistatic, HiE模型),成功破解了物种相互作用中“交互表型可塑性”的完整遗传密码。这项研究成果发表在国际权威期刊《Molecular Ecology Resources》(中科院一区)上,不仅填补了传统数量遗传学的理论空白,更为预测和调控生态系统演化提供了前所未有的计算框架。
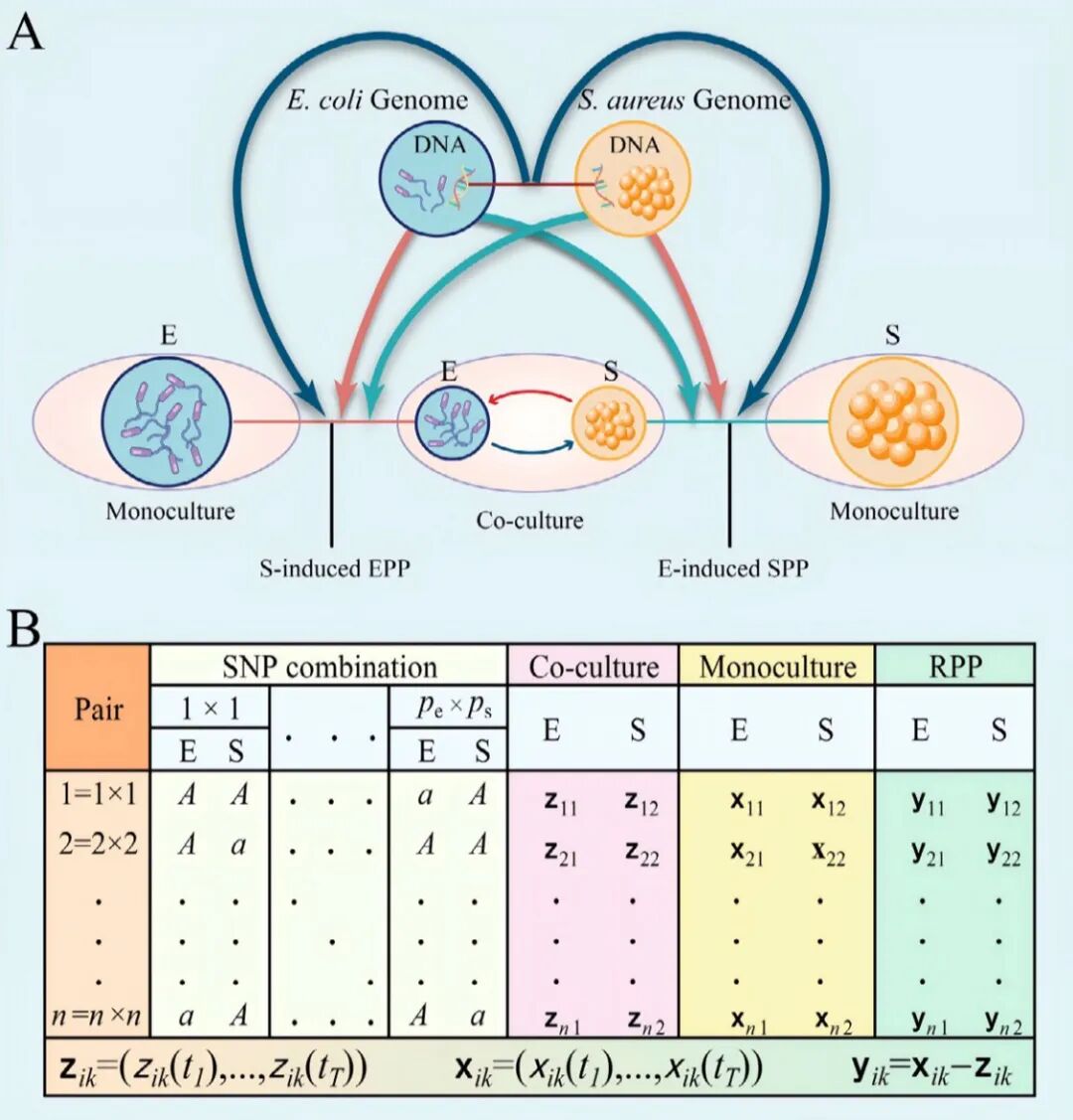
从“单打独斗”到“跨界对话”:遗传学研究的范式革命
传统遗传学研究如同在实验室里研究单个球员的射门技巧——它关注的是一个物种自身的基因如何影响自己的性状。然而,真实的自然界是一场复杂的“足球赛”,每个球员的表现不仅取决于自身能力,更受到对手、队友甚至裁判的实时影响。这种跨物种的基因互作,正是经典理论长期忽视的“遗传盲区”。
邬荣领团队敏锐地指出,在真实的生态群落中,一个物种的表型特征受到三重遗传力量的共同塑造:自身基因的直接调控、共存物种基因的间接影响,以及不同基因组之间的交互作用。研究团队将这种跨基因组的相互作用正式定义为“水平上位性”(horizontal epistasis),并创造性地提出了HiE统计模型。
“这相当于在遗传学中打开了’跨界对话’的维度,”邬荣领教授解释道,“过去我们认为基因只在同一个基因组内部’聊天’,现在我们发现,不同物种的基因之间也在进行跨空间的’通话’,共同决定生态系统的演化方向。”这一概念的提出,标志着数量遗传学从“单基因组研究”迈向“跨基因组协同演化”的关键一跃,为理解生命共同体提供了全新的理论视角。
实验揭秘:大肠杆菌与金黄色葡萄球菌的”基因攻防战”
为了验证HiE模型的强大威力,研究团队设计了一套精巧的微生物“对决”实验。他们选取了100株基因型不同的大肠杆菌(E. coli)和100株金黄色葡萄球菌(S. aureus),构建了这两种常见细菌在单独培养(单培养)和混合培养(共培养)两种环境下的生长对比体系。
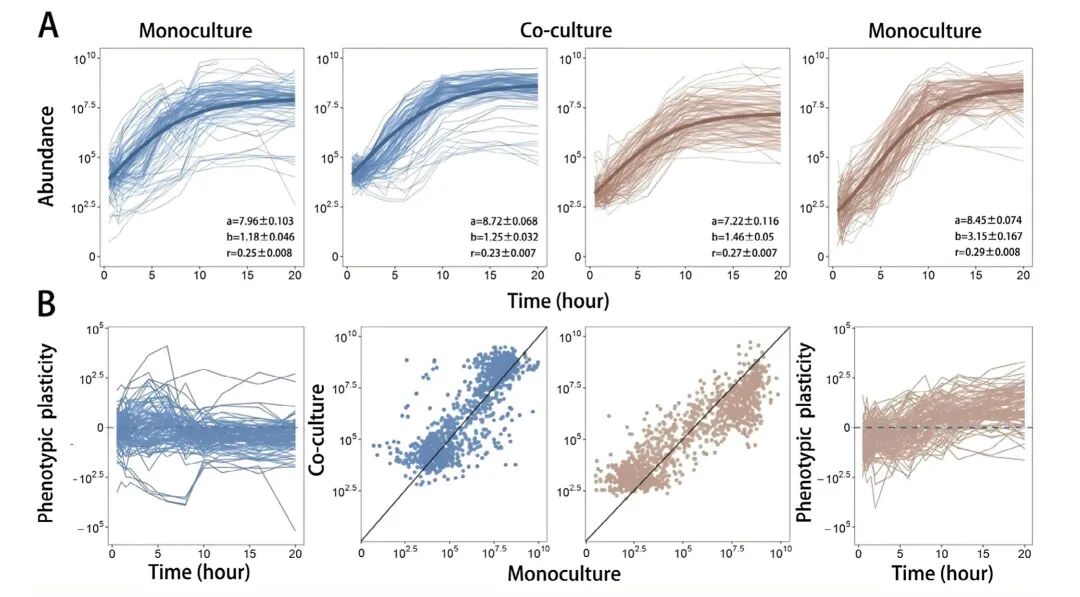
实验结果揭示了一幅高度不对称的“生态遗传图景”,仿佛一场实力悬殊的“基因攻防战”:
进攻与防御的策略差异
研究发现,当与金黄色葡萄球菌共处时,大肠杆菌倾向于激活大量“防御性基因”,一方面强化自身生长能力,另一方面通过少量“进攻基因”抑制对手。而金黄色葡萄球菌则更多依赖“进攻性基因”来应对胁迫,其防御机制相对被动。这种“你攻我守”的非对称策略,解释了为什么在混合培养中,大肠杆菌生长更旺盛,而金黄色葡萄球菌则受到明显抑制。
水平上位性的惊人作用
HiE模型成功识别出超过13万组影响这种相互响应的SNP(单核苷酸多态性)组合。最令人惊讶的是,跨物种的“水平上位性效应”在介导表型可塑性中占据了举足轻重的地位——这在以往的单物种研究中是根本无法观测到的遗传机制。打个比方,这就像发现两支球队的比赛结果不仅取决于各自球员的技术,更取决于双方球员之间“化学反应”的微妙互动。
基因功能的精准定位
通过基因本体论分析,研究团队首次在分子层面绘制了“防御基因”与“进攻基因”的功能图谱。大肠杆菌的防御基因主要集中于小分子生物合成、氨基酸代谢等增强自身活力的通路;而金黄色葡萄球菌的防御基因则与清除外源DNA、抗生素响应等抵抗性机制相关。这种功能分化,完美诠释了两种细菌在生态系统中的不同生存策略。
破解遗传密码:从“单基因”到 “交互式基因组” 的量化解析
HiE模型的核心突破在于,它首次实现了对直接遗传效应、间接遗传效应与水平上位效应的系统性整合与定量解析。这相当于为生态遗传学研究提供了一把“万能标尺”,能够精确测量三种遗传力量的相对贡献。
“我们的模型好比一个基因’窃听器’,”论文第一作者王玉博士形象地比喻,“它不仅能听到每个物种自己基因的表达声音(直接效应),还能捕捉到来自其他物种基因的’隔空喊话’(间接效应),以及不同基因之间的’密谋对话’(水平上位效应)。”
通过对实验数据的深度挖掘,研究团队获得了多项里程碑式发现:
间接遗传效应的颠覆性认知
传统遗传学几乎只关注直接效应,但研究发现,间接遗传效应在生物互作中至少与直接效应同等重要。在金黄色葡萄球菌的表型可塑性中,间接效应甚至超过了直接效应。这意味着,物种的适应性约有一半是“由对手塑造”的。
时间动态变化的精妙调控
遗传效应并非一成不变。在共培养的早期(0-10小时),直接和间接效应的绝对值先升后降,呈现明显的动态调控;而在10小时后,效应强度趋于稳定,但水平上位效应的相对贡献显著提升。这种时序特征揭示了微生物群落从激烈竞争到动态平衡的全过程的遗传基础。
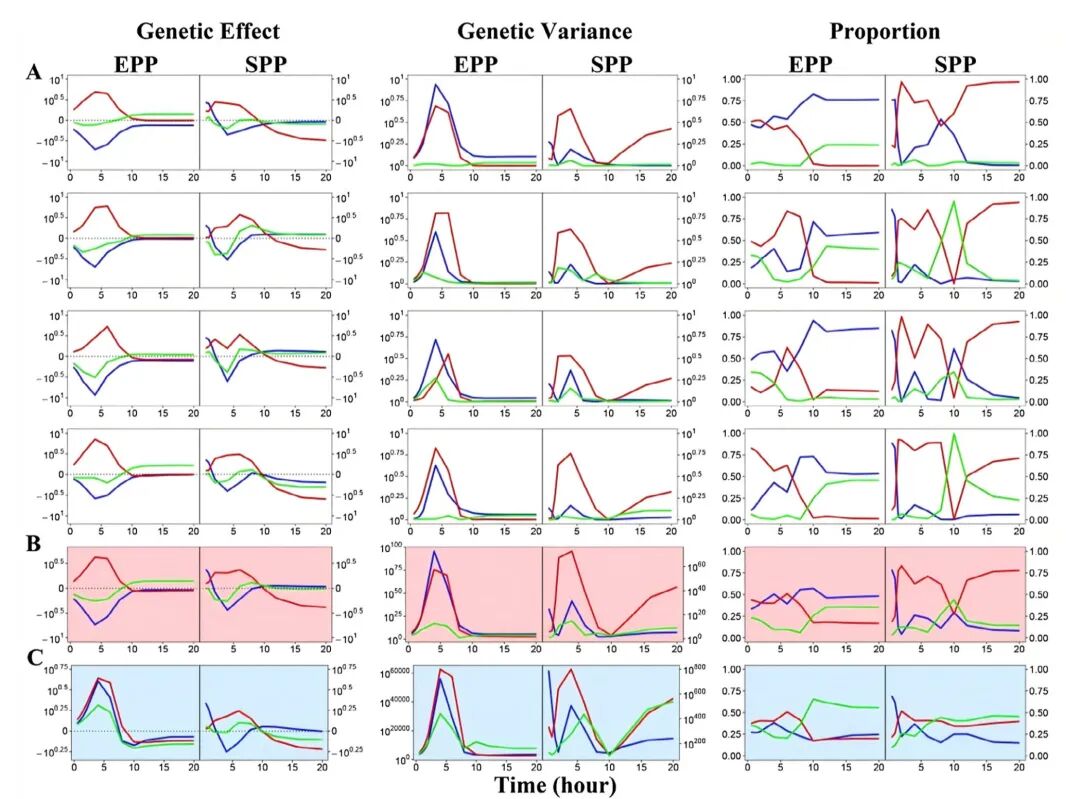
130个核心SNP组合的“双面人生”
研究鉴定出130对两种细菌都有影响的“共通SNP组合”,它们表现出典型的“拮抗性控制”——一个等位基因在增强大肠杆菌适应性的同时,会抑制金黄色葡萄球菌的生长,反之亦然。这就像一把双刃剑,在进化博弈中维持着精妙的平衡。
从理论到应用:重塑微生物组研究与生态预测
这项研究的深远意义远超微生物学范畴。邬荣领团队开创的模型与实验范式,为多个前沿领域打开了全新的可能性:
微生物工程与合成生态
通过精准调控特定防御或进攻基因的表达水平,人类可以“定向编程”微生物群落结构。这对于构建高效的工业发酵体系、修复污染环境的微生物组、乃至设计个性化益生菌治疗方案,都具有直接的指导价值。
抗生素耐药与病原控制
研究揭示了跨物种基因互作对致病性的潜在影响。理解病原菌如何利用进攻基因破坏宿主微生物屏障,或将为对抗耐药菌提供全新靶点。例如,抑制金黄色葡萄球菌的某些进攻基因,可能削弱其致病能力。
生态进化预测
在全球变化背景下,HiE模型为预测群落如何响应环境变化提供了可计算框架。科学家可以模拟不同基因型组合下的群落动态,预判生态系统对气候变暖、入侵物种等胁迫的演化轨迹,为生物多样性保护提供决策支持。
精准医学的新维度
人体本身就是一个超级生态系统。这项研究为理解肠道菌群与宿主、菌群成员之间的基因互作提供了理论工具,未来有望发展出基于”跨界遗传效应”的精准医疗策略。
结语:生命共同体的遗传交响曲
正如邬荣领教授所言:“生命的遗传密码,从来不是孤立书写的——它是在物种之间的相互作用中,被共同塑造、不断演化的。”这项研究以高度原创的理论视角、严谨的数学建模和扎实的实验数据,重新定义了“基因如何在物种互作中发挥作用”这一根本问题。
HiE模型的诞生,不仅填补了传统数量遗传学与进化生物学之间长期存在的空白,更重要的是,它让我们第一次能够量化解读生命共同体的“遗传交响曲”。在这个交响曲中,每个物种既是独奏者,也是伴奏者;它们的基因既在表达自我,也在倾听他者。这种深层次的遗传对话,正是地球生命网络得以维系和演化的根本机制。
随着这一理论工具的推广,人类将有望从“基因-基因”的互动视角,升级到“基因组-基因组”的系统认知,最终实现对生态系统的精准理解、预测与调控。这不仅是一次科学研究的突破,更是人类认识生命、与自然和谐共生的一次重要飞跃。
论文信息
Wang, Y., Zhao, J., He, X., Yang, D., Jin, Y., & Wu, R. (2026). A Computational Ecological Genetic Model of Phenotypic Plasticity in Species Interactions.Molecular Ecology Resources,26(1), e70095.
DOI: https://doi.org/10.1111/1755-0998.70095


