2025年7月9日,上海数学与交叉学科研究院丘成桐院士团队与合作者以“用于神经胶质瘤分割和遗传标记预测的基于最优传输和张量奇异值分解的深度学习模型:一项多中心数据研究(OMT and tensor SVD based deep learning model for segmentation and predicting genetic markers of glioma: a multicenter study)”为题,于国际顶级学术期刊《美国国家科学院院刊》(Proceedings of the National Academy of Sciences of the United States of America,PNAS)(Vol.122, No.28, 2025)发表论文。《美国国家科学院院刊》是国际顶尖综合性期刊,与Nature、Science、Cell并称全球四大综合科学期刊,近五年影响因子为10.6,学科涵盖生物、物理、化学、数学及社会科学,多学科大类排名前5%,对原创性要求极高。
在神经外科临床实践中,胶质瘤的诊断与治疗一直存在诸多挑战。作为最常见的原发性中枢神经系统肿瘤,其高度异质性的生物学特征,使得传统诊疗方法往往力不从心。当前,胶质瘤的临床决策严重依赖术后病理诊断,但侵入性活检可能给患者带来额外风险,且对于位于脑干等关键部位的肿瘤,手术取样往往不可行。因此,神经胶质瘤的术前分级和基因分析对于神经胶质瘤患者的治疗至关重要。
随着医学影像技术和人工智能的发展,基于MRI的多模态影像和组学数据研究成为破解这一困局的利器。然而,目前大多数研究仅涉及有限数量患者,局限于少量样本和数据集来源,无法有效发挥AI模型的效能。此外,现有AI模型在部分数据集上虽表现出不错的预测性能,但无法最有效、最准确地挖掘出多中心影像和基因信息之间的关联,同时缺乏理论上的可解释性,制约了临床应用的可靠性。
为改进现有方法,丘成桐院士团队长期与南京鼓楼医院张冰教授团队开展深度合作,将前沿的计算几何与最优传输理论应用于脑科学领域,实现影像数据的高效处理,并通过创新性代数模型显著提升了深度学习在脑胶质瘤分级与基因分型中的准确性。团队共收集来自16个不同中心的超过3500例脑胶质瘤数据,创新提出最优传输-代数预分类模型(OMT-APC model),使用OMT方法将不规则大脑变换至规则张量,借助密度函数增强影像中肿瘤区域特征,实现高效数据标准化,并完成高精度自适应肿瘤分割,这对于多中心任务来说至关重要。研究团队进一步突破传统方法局限,基于多模张量奇异值分解,创新性地将代数方法与深度学习模型相融合,在图像模型基础上加入张量代数特征,显著提升了模型识别肿瘤和基因分型的能力。
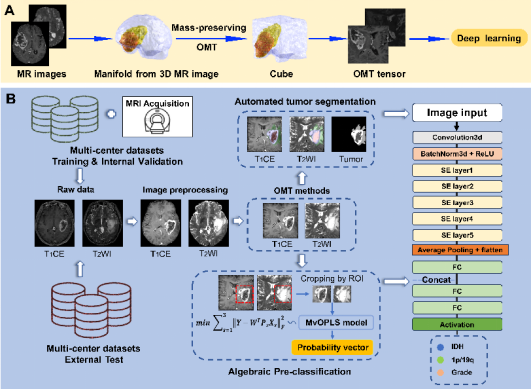
(A) OMT处理脑影像. (B) 研究流程图.
研究成果显示,通过在多中心数据上进行模型训练,OMT-APC模型在标准测试集TCGA上的胶质瘤分级、IDH突变状态、1p/19q共缺失分类精度分别能够达到85.5%、91.7%和80.9%,相比以往的方法,分类精度分别能够提升1.5%、7.7%和4.9%。在应用层面,该模型为不适合进行肿瘤切除手术、仅需钻孔活检进行诊断的患者,提供了一种高精度的非侵入性替代方案,在无创条件下帮助患者获取胶质瘤基因信息。此外,当样本误差导致诊断结果不明确时,OMT-APC方法可作为组织学结果的额外核查手段,为医生提供辅助诊断依据。
研究成果在胶质瘤分析和临床应用上展现出良好的潜力。目前成果相关算法软件已在南京鼓楼医院影像科布置并参与临床检验,其影像处理效果与分析精度均得到影像科医生一致认可。经医生检验,临床测试超过86%的病例WT分割精度超95%,TC分割精度超90%,为多中心医学影像临床分析提供了新的研究范式和技术支撑,也为“数学+AI”研究医学应用问题提供了全新的研究思路。
南京应用数学中心及上海数学与交叉学科研究院工程师王瀚、东南大学李铁香教授、台湾师范大学黄聪明教授以及南京鼓楼医院医生朱正阳、杨惠泉、陶震楠为论文第一作者,上海数学与交叉学科研究院理事长丘成桐院士、南京应用数学中心及上海数学与交叉学科研究院林文伟教授以及南京鼓楼医院张鑫、张冰医生为论文通讯作者。研究得到了科技创新2030 —“脑科学与类脑研究”重大项目、国家自然科学基金、国家科学及技术委员会(台湾)、江苏省应用数学科学研究中心、南京鼓楼医院医学发展医疗救助基金会资助项目、南京鼓楼医院2023年临床研究专项资金项目面上项目和上海数学与交叉科学研究院的支持。
论文链接: https://doi.org/10.1073/pnas.2500004122

